【学术争鸣】血管正性重构与血管管腔扩张性重构两种不同现象的区分
文章来源:中国脑血管病杂志, 2023, 20(3):200-204.
作者:刘文波 唐垚 郭德华 何艳艳 丁乾昊 马驰 贾茹峰 李天晓 贺迎坤
基金项目:河南省中青年卫生健康科技创新人才培养项目(YXKC2020041);河南省医学科技攻关计划省部共建青年项目(SBGJ202003004);河南省高等学校重点科研项目(21A320002)
通信作者:贺迎坤,Email:heyingkun@ zzu.edu.cn
动脉粥样硬化是引起心脑血管类疾病的重要原因[1-3],是一个动态演变过程,严重时可形成斑块造成血管狭窄,一部分患者病变处血管发生代偿性扩张以延缓管腔狭窄进展,即外弹力膜(external elastic membrane, EEM)的横断面面积(cross-sectional area,CSA)增大的现象,称为“正性重构”[4-5]。这一现象与血管斑块负荷逐渐增大有关,斑块过大会变得不稳定且破裂风险增高,与临床缺血事件的发生密切相关[6-11]。近年来,随着血管内治疗广泛应用于冠状动脉、颅内动脉粥样硬化性狭窄的治疗当中,研究显示,部分患者介入术后随访时,病变部位不但未发生管腔的再狭窄,甚至出现管腔扩张的现象[12-15]。这种现象可能与病变处的斑块消退、夹层修复、管壁重构相关[15-19]。有研究认为,这种现象能提高患者血流灌注量,可能有利于预防再发卒中,改善患者预后[12,15,20]。但目前对这一现象并无明确定义,部分相关研究习惯以正性重构对其进行描述。结合本中心以往的经验,如果将随访时管腔扩张这一现象称为正性重构,易将其与缺血事件联系到一起。因此我们提出“血管管腔扩张性重构”这一概念,希望能够帮助进行区分和描述,有助于后续开展与其相关的研究。
1 血管正性重构
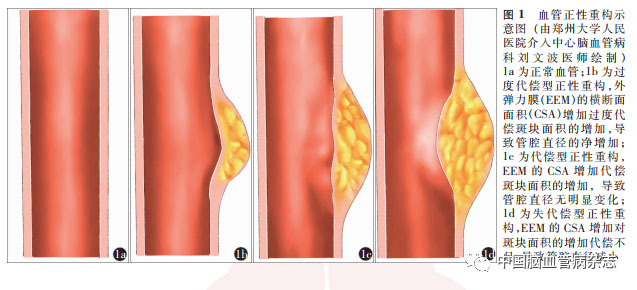
1987年Glagov 等[4]通过对136 例人体进行尸检,最早发现了心脏左主干的血管重构现象,即在动脉粥样硬化的进展早期,随着斑块体积增加,EEM的CSA发生相应的代偿性扩大,以取代斑块所占据的管腔面积,从而保证血流不会显著减少,但当斑块负荷超过EEM的CSA的40%时,这种代偿将无法继续维持,进而造成血管管腔的狭窄,血流量下降。由此可见,血管重构是一个动态的演变过程,这一现象后来被称为Glagov现象[21]。2001 年美国心脏病学会发布的关于血管内超声的专家共识对正性重构和负性重构进行定义,用重构指数(remodeling index,RI)来描述重构的程度及趋势,RI 为病变处EEM的CSA与参考处EEM的CSA比值,将RI > 1定义为正性重构,RI < 1定义为负性重构(血管内超声不能识别内弹力膜)[5]。之后的相关研究多以该共识的定义来界定正性重构和负性重构,仅在临界值上有所不同。现有研究多将RI > 1.05 定义为正性重构,< 0. 95 定义为负性重构,0. 95 ~ 1. 05 定义为中间性重构[22-23]。考虑到外表正常的参考血管可能存在血管重构的可能,因而不采用1 为界值[22]。关于冠状动脉正性重构的研究认为,这种现象有增加斑块破裂的风险,与临床缺血事件的发生密切相关[9-10]。血管内超声在冠状动脉领域被广泛应用于检查血管壁以及动脉粥样硬化斑块的情况,但由于颅内血管结构复杂,其在颅内的应用依然少见。近来随着高分辨率磁共振的出现,使对颅内动脉的管壁结构和动脉粥样硬化斑块的观察成为可能,从而对患者病情进行有效的评估[24-27]。在评价正性重构时,高分辨率磁共振和血管内超声方面的研究有着基本相同的观点。关于高分辨率磁共振在颅内动脉应用的研究显示,正性重构的颅内动脉同样具有易于发生斑块破裂和继发卒中的风险,计算上也采用1. 05作为临界值,但是为了简化分组,有些研究不再划分中间性重构组,而是将RI≥ 1. 05定义为正性重构,将RI < 1. 05 定义为非正性重构[7,28-29]。因冠状动脉CT血管成像有高估RI的倾向,也有研究以1.10作为临界值,如Gauss等[30]提出了正性重构为RI≥1. 10,即病变处EEM的CSA较参考处EEM的CSA平均值增加10%。与以RI≥ 1.05 为参考标准相比,Gauss等[30]的研究中,RI≥ 1. 10 预测血管正性重构的敏感度降低(83%比100%),但特异度增加(78%比45%)。目前对于血管重构的分类尚无统一标准,相关研究中分类划分仍较混乱。结合Glagov现象和正性重构的影像学定义,我们推测血管正性重构,即病变处EEM的CSA增大时,动脉管腔会随着斑块的进展而发生变化,是一种动态变化的过程,可能会出现过度代偿、代偿、失代偿等不同阶段(图1)。
2 血管管腔扩张性重构
血管内介入成形术治疗冠状动脉、颅内动脉粥样硬化性狭窄患者术后的影像随访结果显示,有一部分患者病变部位的管腔出现了相较于术后即刻(指手术治疗性操作之后,在结束手术之前,最后一次行造影观察病变部位的时刻)的扩张,这种现象的出现可提高患者血流灌注量,可能有利于预防再发卒中,改善患者预后[12,15,20],且该现象常出现在药物球囊治疗患者的术后随访当中[13-14,31]。对于这一现象,目前尚无明确的定义,部分相关研究将其称为“血管正性重构”,但如果仔细比较该现象与血管正性重构的概念不同。如前文所述,血管正性重构指的是动脉粥样硬化发展过程中,病变处血管EEM的CSA较病变远、近端参考处EEM的平均CSA增大。而在血管内介入成形术治疗动脉粥样硬化性狭窄后影像随访时出现管腔扩张的患者中,测量和对比的指标是病变部位随访时管腔的狭窄率与术后即刻管腔狭窄率,这与正性重构的测量与对比指标RI 不同。虽然两者可能存在联系,但将血管正性重构这一概念用于描述随访时血管管腔相对于术后即刻扩张这一现象,显然不够准确。为了能够明确对这一现象的描述,我们在本研究中提出“血管管腔扩张性重构”这一概念,并将其定义为:在动脉粥样硬化性狭窄患者血管内介入成形术后的影像随访中,病变部位管腔最狭窄处的狭窄率相较于术后即刻狭窄率减少大于10% [14,31-32],并将病变部位管腔最狭窄处的狭窄率相较于术后即刻狭窄率增加大于10%定义为“血管管腔缩窄性重构”,介于二者之间者定义为“血管管腔无重构”。狭窄率的计算采用症状性颅内动脉疾病华法林-阿司匹林研究(Warfarin-Aspirin symptomatic intracranial disease study, WASID)方法[33],即狭窄率=(1 - Ds/ Dn)× 100%(Dn、Ds分别代表正常处和最狭窄处管腔直径,前者一般为狭窄处近心端管腔直径,若近心端有狭窄,则考虑狭窄处远心端)。考虑到在上述的血管正性重构现象中,血管管腔面积与EEM 的CSA 变化过程的不一致性,我们推测在发生管腔扩张性重构时,即病变部位管腔最狭窄处狭窄率较术后即刻减少的情况下,病变处血管EEM的CSA也可能会出现3种情况,根据这3种情况我们对管腔扩张性重构进行了以下3种划分(图2),即:血管正性重构型管腔扩张性重构、血管中间性重构型管腔扩张性重构、血管负性重构型管腔扩张性重构。
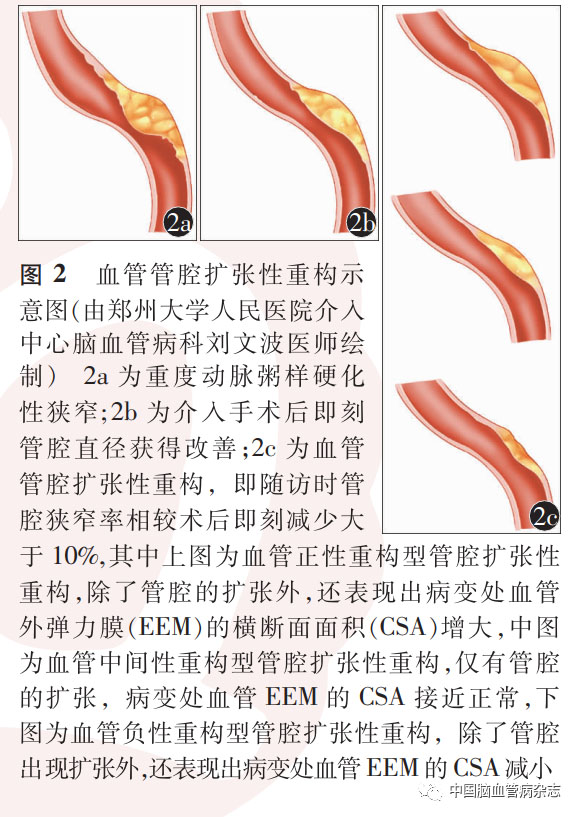
(1)血管正性重构型管腔扩张性重构:同时合并有血管正性重构和管腔扩张,即随访时除了管腔的扩张外,还表现出病变处血管EEM的CSA增大;(2)血管中间性重构型管腔扩张性重构:随访时仅有管腔的扩张,病变处血管EEM的CSA接近正常。(3)血管负性重构型管腔扩张性重构:随访时合并有血管负性重构和管腔扩张,即在随访时,除了管腔出现扩张外,还表现出病变处血管EEM的CSA减小。已有关于药物球囊治疗颅内动脉粥样硬化性狭窄的高分辨率磁共振研究结果显示,在随访时会出现病变部位管壁斑块的修饰与稳定,以及管壁厚度的减小[17]。因此我们考虑上述血管管腔扩张性重构的后两种情况可能为斑块的消退所致,造成EEM向正常方向恢复,甚至由于斑块消退过多,造成EEM的塌陷。然而具体机制仍有待考证,需要进一步研究明确。有研究显示,灌注降低是卒中复发的重要危险因素[34],由于扩张的管腔能够提高血流灌注量,结合以往文献中管腔扩张能够减少缺血事件发生的证据[20],因此我们推测发生血管管腔扩张性重构的这部分患者将更有可能从血管成形术中获益。
从上述的描述中,我们能看出,血管正性重构和血管管腔扩张性重构指的是不同的现象。我们希望通过此文,可以让读者区分这两种现象,在临床及科研工作中更准确地对其进行描述,也希望未来有更多关于血管管腔扩张性重构的研究,以进一步探索其发生机制,为临床治疗提供相关指导。

扫描二维码,可用手机阅读此文章

 互联智慧分诊平台
互联智慧分诊平台
 在线问诊
在线问诊 信息查询
信息查询